Badanie poziomu kalprotektyny w kale cieszy się coraz większą popularnością zarówno w środowisku medycznym, jak i wśród pacjentów. Wynika to nie tylko z łatwości wykonania oznaczenia, ale także z faktu, że badanie to jest bezbolesnosne oraz nie wymaga konieczności stosowania diety i przygotowania przed badaniem. Badanie stężęnia kalprotektyny ma praktyczne zastosowanie w diagnostyce różnicowej nieswoistych chorób zapalnych jelit i zespołu jelita drażliwego oraz monitorowaniu aktualnego stanu zdiagnozowanej już IBD. Badanie to w określonych sytuacjach pozwala zmniejszyć liczbę wykonywanych kolonoskopii, oszczędzając pacjentom dodatkowego stresu.
Stężęnie kalprotektyny w kale – norma
Górna granica normy stężenia kalprotektyny w kale u dorosłych została przyjęta jako 50 µg/g i jest sugerowana przez większość producentów testów diagnostycznych. Poniżej przedstawiono proponowany algorytm diagnostyczny z zastosowaniem badania stężenia kalprotektyny w kale, który pozwala na ukierunkowanie dalszej diagnostyki.
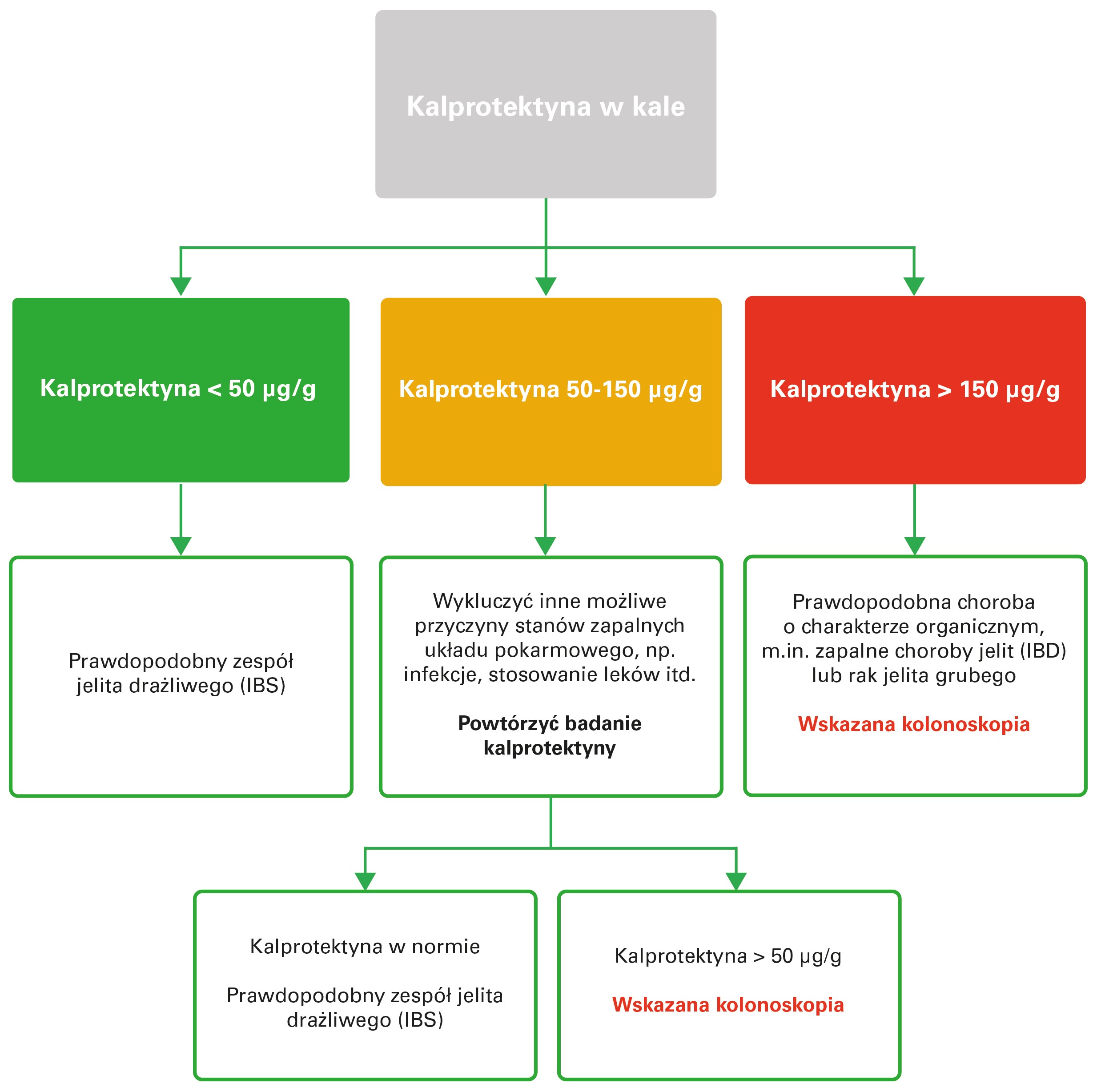
Ryc. 1. Algorytm diagnostyczny.
Na podstawie: R.A. Sherwood, Faecal Markers of Gastrointestinal Inflammation. Journal of Clinical Pathology 2012; 65 (11): 981–985.
Inne zastosowania oznaczania stężęnia kalprotektyny w kale
Badanie stężęnia kalprotektyny w kale znalazło wiele zastosowań:
- Monitorowanie aktywności choroby
- Ocena odpowiedzi na leczenie
- Ocena nawrotu pooperacyjnego
Chcesz wiedzieć więcej na ten temat? Zapoznaj się z artykułem:
KLIKNIJ
Literatura:
- Ayling R.M., Kok K., Fecal calprotectin. Advances in Clinical Chemistry 2018; 87: 161–190.
- ASGE Standards of Practice Committee, Fisher D.A., Maple J.T., Ben-Menachem T., Cash B.D., Decker G.A., Early D.S. et al., Complications of colonoscopy. Gastrointestinal Endoscopy 2011; 74 (4): 745–752.
- Sherwood R.A., Faecal Markers of Gastrointestinal Inflammation. Journal of Clinical Pathology 2012; 65 (11): 981–985.
- Waugh N., Cummins E., Royle P., Kandala N.B., Shyangdan D., Arasaradnam R., Faecal calprotectin testing for differentiating amongst inflammatory and non-inflammatory bowel diseases: systematic review and economic evaluation. Health Technology Assessment 2013; 17 (55): 1–211.
- Chen J.M., Liu T., Gao S., Tong X.D., Deng F.H., Nie B., Efficacy of noninvasive evaluations in monitoring inflammatory bowel disease activity: A prospective study in China. World Journal of Gastroenterology 2017; 23 (46): 8235–8247 [PMID: 29290660 DOI: 10.3748/wjg.v23.i46.8235].
- Sipponen T., Kolho K.L., Fecal calprotectin in diagnosis and clinical assessment of inflammatory bowel disease. Scandinavian Journal of Gastroenterology 2015; 50 (1): 74–80.
- Annese V. et al., European evidence based consensus for endoscopy in inflammatory bowel disease. Journal of Crohn’s and Colitis 2013; 7 (12): 982–1018.
- Kolho K., Raivio T., Lindahl H., Savilahti E., Fecal calprotectin remains high during glucocorticoids therapy in children with inflammatory bowel disease. Scandinavian Journal of Gastroenterology 2006; 41 (6): 720–725.
- Olender K., Bergmann K., Odrowąż-Sypniewska G., Kalprotektyna w kale jako marker zapalny w nieswoistych zapaleniach jelit. Diagnostyka Laboratoryjna 2012; 48 (4): 433–439.
- Gisbert J.P., Bermejo F., Perez-Calle J.L. et al., Fecal calprotectin and lactoferrin for the prediction of inflammatory bowel disease relapse. Inflammatory Bowel Diseases 2009; 15 (8): 1190–1198.

Lubie ten portal